OKSYDAZA GLUKOZOWA
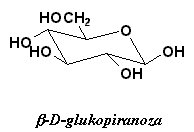
Oksydaza glukozowa jest to enzym, który spośród np. 64 różnych cyklicznych form 16 aldoheksoz (cukrów), katalizuje utlenianie tlenem powietrza praktycznie tylko jednej z form glukozy; jest nią β-D-glukopiranoza:

C6H12O6 + O2 + H2O → C6H12O7 + H2O2 (1)
(produktem utleniania glukozy jest kwas glukonowy, równanie tej reakcji jest w rzeczywistości znacznie bardziej F skomplikowane; patrz pod koniec tego opracowania)
PASKOWY TEST MEDYCZNY
Ogromna specyficzność tego enzymu znalazła zastosowanie w podręcznych testach służących do szybkiego, półilościowego oznaczania stężenia glukozy np. w moczu. Do doświadczeń użyto testu "MULTISTIX". Jest to wąski plastikowy pasek, na którym naklejone są niewielkie pola z porowatego materiału, nasycone odpowiednimi odczynnikami, służące do oznaczeń wielu parametrów medycznych. Ostatnie po lewej stronie, oznaczone gwiazdką * pole służy do pomiaru stężenia glukozy. Porowata masa zawiera oksydazę glukozową. Po zanurzeniu testu 2 w roztworze zawierającym glukozę, w wyniku reakcji z tlenem powstaje nadtlenek wodoru. Do jego wykrycia stosuje się po prostu jodek potasu KI. W wyniku reakcji nadtlenku wodoru z KI, powstaje brunatny jod:
H2O2 + 2 I− + 2 H+ → I2 + 2 H2O (2)

Ponieważ ilości tworzącego się nadtlenku wodoru są bardzo niewielkie, dlatego reakcja utleniania jodku do jodu jest bardzo powolna. Do jej przyspieszenia używa się drugiego enzymu: F peroksydazy. Maleńkie pole na plastikowym pasku jest więc skomplikowanym laboratorium: oksydaza glukozowa rozpoznaje glukozę i powoduje powstanie nadtlenku wodoru w ilości proporcjonalnej do ilości glukozy. Do wykrycia nadtlenku wodoru służy jodek potasu. Do przyspieszenia tej ostatniej reakcji służy drugi enzym: peroksydaza. Całość zabarwiona jest zielonym neutralnym barwnikiem, który ułatwia porównywanie barwy. (Dla porównania umieszczono zdjęcie 1 paska zanurzonego w czystej wodzie). Stężenie glukozy odczytuje się przez porównanie z załączoną skalą barw:

PAKIET ANTYOKSYDACYJNY
W reakcji (1) zostaje zużywany gazowy tlen. Reakcja ta została wykorzystana do produkcji bardzo pomysłowego i całkowicie nieszkodliwego urządzenia służącego do pochłaniania tlenu wewnątrz opakowań z produktami spożywczymi wrażliwymi na szkodliwe działanie tlenu: orzeszków ziemnych, mleka w proszku, puszkowanego masła itp. Pakiet antyoksydacyjny jest to torebeczka z folii plastikowej przepuszczalnej dla gazów, zawierająca granulowaną wilgotną mieszaninę glukozy oraz oksydazy glukozowej. W wyniku reakcji zostaje powoli zużywany tlen. Powstają jednak równocześnie dość znaczne ilości nadtlenku wodoru, który w większym stężeniu może powodować dezaktywację oksydazy glukozowej. Aby do tego nie dopuścić, do pochłaniacza dodaje się niewielką ilość enzymu (jest nim katalaza) powodującego rozkład tworzącego się nadtlenku wodoru:
2 H2O2 → O2 + 2 H2O (3)
Uważny Czytelnik powinien zgłosić wątpliwość: w reakcji (1) gazowy tlen zostaje co prawda zużywany, natomiast katalityczny rozkład (3) nadtlenku wodoru powoduje ponowne wytwarzanie gazowego tlenu! Do wyjaśnienia tego pozornego paradoksu wystarczy zapisać równania (1) oraz (3) w taki sposób, aby współczynniki przy H2O2 były identyczne, a następnie oba równania zsumować.
ANALIZA SKŁADU POWIETRZA
Skuteczność opisywanego pochłaniacza tlenu proponuję zademonstrować następująco. Do dna suchego cylindra miarowego 100 ml wprowadzić, zgiętą lekko torebeczkę-pakiet (świeżo wyjęty z opakowania z np. orzeszkami ziemnymi). Do dna cylindra wprowadzić również cienki wężyk plastikowy, a następnie odwrócony do góry dnem cylinder wraz z wężykiem zanurzyć w naczyniu z wodą ("wanienka pneumatyczna"). Wyssać ustami tyle powietrza, aby poziom wody wewnątrz cylindra ustalić dokładnie na "100 ml" i wężyk usunąć. Po 1,5-2 dobach odczytać objętość pozostałego gazu (azotu) w cylindrze; jest ona równa ok. 80 ml.
LITERATURA
T.Pluciński. "Doświadczenia chemiczne" . Wyd. „Adamantan”, Warszawa 1997, s. 94. [Oksydaza
glukozowa]
Tomasz Pluciński
nowy adres:
tomasz.plucinski@ug.edu.pl
| F | strona główna |